এইচএসসিতে রসায়ন পড়ার সময় জৈব রসায়ন (Organic Chemistry) অধ্যায়ের নাম শুনে ভয় পায়নি, এমন মানুষ খুঁজে পাওয়াটা একটু কষ্টকর। বিশাল বিশাল রাসায়নিক বিক্রিয়া ও সমীকরণ, তাদের হাজারো ব্যাখ্যা, শত শত যৌগের সমাহার আর বইয়ের পৃষ্ঠার পর পৃষ্ঠা- জৈব রসায়ন এর কথা শুনলে আমাদের মাথায় এগুলোই সবার আগে আসে। অনেক শিক্ষার্থীই রসায়ন বইতে জৈব যৌগ অধ্যায়ের দীর্ঘ এই আলোচনা দেখে অনেক হতাশ হয়ে পড়ে। কিন্তু আসলে এতটাও কঠিন না এই জৈব রসায়ন, বরং একটু মনোযোগ দিয়ে বুঝে বুঝে পড়তে পারলে জৈব রসায়নই হতে পারে একজন শিক্ষার্থীর ভালো ফলাফল করার জন্য সবচেয়ে বড় অস্ত্র।
জৈব যৌগ কাকে বলে?
হাইড্রোজেন ও কার্বন দ্বারা গঠিত হাইড্রোকার্বন এবং হাইড্রোকার্বন থেকে উদ্ভূত যৌগসমূহকে জৈব যৌগ বলে। জৈব যৌগ বা জৈব পদার্থ কাকে বলে এটা জানার পর মানুষের মনে জৈব পদার্থের উৎস নিয়ে কৌতূহল সৃষ্টি হতে থাকে। সুইডিশ বিজ্ঞানী বার্জেলিয়াস ১৮১৫ সালে প্রস্তাব করেন যে, জৈব যৌগসমূহ কেবল সজীব উদ্ভিদ ও প্রাণীদেহে এক রহস্যময় প্রাণশক্তির প্রভাবে উৎপন্ন হয়ে থাকে। একে প্রাণশক্তি মতবাদ বলে। ১৮২৮ সালে ফ্রেডরিক উলার পরীক্ষাগারে অজৈব অ্যামোনিয়াম ক্লোরাইড ও লেড সায়ানেট থেকে আকস্মিকভাবে ইউরিয়া প্রস্তুত করে প্রাণশক্তি মতবাদ ভুল প্রমাণ করেন।
জৈব যৌগের সংখ্যা ৮০ লক্ষের অধিক। অন্যদিকে অজৈব যৌগের সংখ্যা প্রায় ১ লক্ষের মত। এই সংখ্যাধিক্যের কারণ হলো – কার্বন মৌলের ক্যাটেনেশন ধর্ম, জৈব যৌগের সমাণুতা ধর্ম, জৈব যৌগের পলিমারকরণ, কার্বনের তড়িৎ ঋণাত্মকতা ও বন্ধন শক্তি।
অনেক সময় দেখা যায়, জৈব রসায়নের অনেক ছোট ও সহজ টপিকগুলো বইয়ের পাতায় অনেক বড় করে বর্ণনা করা থাকে। এটি একদিকে যেমন সময়সাপেক্ষ, অন্যদিকে এসব টপিক বুঝতেও কিছুটা বেগ পেতে হয়।
জৈব রসায়ন এর ভয় আমাদেরকে উপরের ছবির মতই বিব্রতকর অবস্থায় ফেলতে পারে। জৈব রসায়ন এর প্রতি এই ভয় কাটিয়ে উঠতে চাইলে যে ৫টি বিষয় না জানলেই নয়, সেগুলো আয়ত্তে আনার জন্য রয়েছে নিচের কয়েকটি সহজ নিয়ম ও কিছু শর্টকাট:
১. ইলেক্ট্রোফাইল-নিউক্লিওফাইল নির্ণয়ন:
“কোনটা ইলেক্ট্রোফাইল, কোনটা নিউক্লিওফাইল, কিছুই তো বুঝতে পারছি না।”
সত্যি বলতে, ইলেক্ট্রোফাইল ও নিউক্লিওফাইল চিহ্নিত করা অনেক সহজ একটা ব্যাপার, যতটা না কঠিন করে আমরা চিন্তা করে থাকি। পজিটিভ-নেগেটিভের মারপ্যাচটা একবার ধরতে পারলেই ইলেক্ট্রো-নিওক্লিওফাইল ঘায়েলের ক্রিপ্টোনাইটটা আমাদের হাতের মুঠোয় চলে আসা সময়ের ব্যাপার। কিভাবে? দেখে আসা যাক-
ফাইল শব্দের অর্থ ভালবাসা। এতটুকু জানা থাকলেই আমরা নিজেরাই বুঝতে পারি, ইলেক্ট্রোফাইল কি আর নিওক্লিওফাইল কি। নাম শুনেই বুঝতে পারছি যে, ইলেক্ট্রোফাইল হলো ইলেকট্রনপ্রেমী ও নিওক্লিওফাইল হলো নিউক্লিয়াসপ্রেমী। আমরা ইতিমধ্যে পড়েছি যে, ইলেক্ট্রনের চার্জ ঋণাত্মক ও নিউক্লিয়াসের (প্রোটন-নিউট্রন) চার্জ ধনাত্মক।
এখন মনে করো, তুমি মার্সিডিজ বেঞ্জ কোম্পানির বিরাট ভক্ত। তোমার অনেকদিন ধরে ধূসর রঙের একটা মার্সিডিজ এএমজি গাড়ি কেনার ইচ্ছা রয়েছে। মার্সিডিজ গাড়ির প্রতি তোমার এই চাহিদার মানে হলো, তোমার গ্যারেজে ঐ নির্দিষ্ট মডেলের গাড়িটা অনুপস্থিত বা ঘাটতি বিদ্যমান। ঠিক এইরকমই হলো ইলেক্ট্রোফাইল ও নিউক্লিওফাইল। ইলেক্ট্রোফাইল ইলেকট্রনপ্রেমী হওয়ায় তার নিজের কাছে ইলেকট্রনের ঘাটতি রয়েছে। ইলেকট্রনের প্রতি ইলেক্ট্রোফাইলের এই চাহিদা তাকে ধনাত্মক করে তুলে। জেনে রাখা ভাল যে, ধনাত্মক কোনো পদার্থ সর্বদা ঋণাত্মক পদার্থকে লাভ করতে চায়। অন্যদিকে, নিওক্লিওফাইল যেহেতু প্রোটন-নিউট্রনের ধনাত্মক ধর্মের ভক্ত, সুতরাং তারা নিজেরা ঋণাত্মক।
শর্টকাট: ইলেক্ট্রোফাইলের ক্ষেত্রে,
তুমি = ইলেক্ট্রোফাইল
মার্সিডিজ গাড়ি = ইলেকট্রন
মার্সিডিজ গাড়ির প্রতি তোমার আকাঙ্ক্ষা = ইলেকট্রনের প্রতি ইলেক্ট্রোফাইলের আকাঙ্ক্ষা
এবার একইভাবে নিউক্লিওফাইলের শর্টকাটও নিজেরাই বের করে নিতে পারবো আমরা।
কোর্সটিতে যা যা পাচ্ছেন:
HSC 2025 অনলাইন ব্যাচ (ফিজিক্স, কেমিস্ট্রি, ম্যাথ, বায়োলজি)
২. অ্যালকিন ও অ্যালকাইনের বিক্রিয়ার সাদৃশ্যতা:
জেনে রাখা ভাল যে, অ্যালকিন ও অ্যালকাইন- এই ধর্মের যৌগগুলো অধিকাংশ বিক্রিয়ায় একই রকমের আচরণ করে থাকে। মূলত এরা অন্য কোনো যৌগের সাথে সংযোজন ও বিয়োজন বিক্রিয়ায় অংশ নিয়ে সাদৃশ্যপূর্ণ আচরণ করে। যেমন: (ইথিন) কে HBr (হাইড্রোজেন ব্রোমাইড) এর সাথে যুক্ত করলে ইথিনের একটি বন্ড ভেঙ্গে যাবে, সাথে সাথে যুক্ত হবে একটি কার্বনের সাথে ও যুক্ত হবে অন্য কার্বনটির সাথে।
অ্যালকাইনের ক্ষেত্রেও একই ধরনের বিক্রিয়া দেখা যায়। একই বিক্রিয়াতে ইথাইন () এর সাথে হাইড্রোজেন ব্রোমাইড বিক্রিয়া করলে কার্বনের একটি পাই বন্ধন ভেঙ্গে একটি কার্বনের সাথে হাইড্রোজেনের ধনাত্মক অংশটি এবং অন্য কার্বনের সাথে ব্রোমাইডের ঋণাত্মক অংশটি যুক্ত হবে।
শর্টকাট: অ্যালকিন ও অ্যালকাইনের একটি বন্ধন ভেঙ্গে যাবে এবং অপর বিক্রিয়কের ধনাত্মক ও ঋণাত্মক অংশগুলো কার্বনের সাথে নতুন বন্ধন গঠন করবে।
৩. কার্যকরী মূলকের ডিগ্রী:
জৈব রসায়নের শুরুর দিকে অনেক সময় দেখতে পাবে জৈবের নামের পূর্বে ডিগ্রী লেখা থাকে এবং তারপর যৌগের কার্যকরী মূলকের নাম থাকে, যেমন ১, ২,৩ অ্যালকোহল। পরীক্ষার প্রশ্নে একটা যৌগের রাসায়নিক সংকেত দিয়ে যৌগটির কার্যকরী মূলক কত ডিগ্রী তা জানতে চাওয়া হতে পারে। অনেক সময় দেখা যায় এই ছোট প্রশ্নটির উত্তর দিতে দিতে আমাদের অনেকটা সময় চলে যায়। কিন্তু কার্যকরী মূলকের ডিগ্রী বের করার একটা সহজ পদ্ধতি রয়েছে।
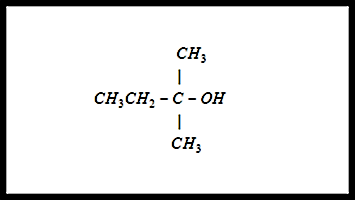
উপরের যৌগটি একটি অ্যালকোহল, কেননা এই যৌগে কার্যকরী মূলক হিসেবে OH বা হাইড্রক্সিল মূলক রয়েছে। এখন এই যৌগটির কার্যকরী মূলকের ডিগ্রী বের করার জন্য প্রথমেই আমরা দেখবো যে OH মূলক টা কোন কার্বনের (C) সাথে যুক্ত এবং সেই কার্বনের সাথে আর কতটি কার্বন সরাসরি সংযুক্ত। দেখা যাচ্ছে, OH মূলক যেই কার্বনের সাথে সংযুক্ত, সেই কার্বনের সাথে আরো ৩টি কার্বন যুক্ত রয়েছে। তাই এই যৌগের ক্ষেত্রে কার্যকরী মূলকটির ডিগ্রী ৩ এবং এটি একটি ৩° অ্যালকোহল। এখন বলে রাখা ভালো যে, একদম মাঝ বরাবর যেই কার্বনটি রয়েছে, তার সাথে ঠিক বাম পাশে CH3CH2 রয়েছে। কিন্তু মাঝের কার্বনটি সরাসরি শুধুমাত্র বামপাশের CH2 এর সাথে যুক্ত। যৌগের সাথে চার্জ কিংবা ফ্রি রেডিক্যাল (মুক্ত অণু-পরমাণু-আয়ন) দেয়া থাকলেও নিয়মটা একই। দেখতে হবে যে, সেই চার্জ যেই কার্বনের সাথে যুক্ত, সেই কার্বন অন্য কতটি কার্বনের সাথে সরাসরি যুক্ত।
দেখা যাচ্ছে, CH এ একটি ধনাত্মক চার্জ বিদ্যমান। সুতরাং চার্জ সম্বলিত কার্বনটি CH2 ও CH3 এর সাথে সরাসরি যুক্ত। তাই এটি হবে ২°-কার্বো ক্যাটায়ন।
শূন্য ডিগ্রী বলতে কিছু নেই, শূন্য ডিগ্রীর বদলে বলা হয় মিথাইল। অর্থাৎ কোনো যৌগের ডিগ্রী শূন্য হলে তা মূলত একটি মিথাইল।
শর্টকাট: কার্যকরী মূলকটি যে কার্বনে যুক্ত, সেই কার্বনটি আর কতটি কার্বনের সাথে ‘সরাসরি ‘ সংযুক্ত।
৪. যৌগের রূপান্তর :
রাসায়নিক বিক্রিয়ার মাধ্যমে এক যৌগ থেকে অন্য যৌগ তৈরি করাই মূলত জৈব যৌগের রূপান্তর বা Conversion of Organic Elements নামে পরিচিত। অনেক সময় দেখা যায়, প্রদত্ত উৎপাদ সরাসরি বিক্রিয়ক থেকে উৎপন্ন করা যায় না। তখন ধাপে ধাপে আরো অনেক যৌগ উৎপন্নের মাধ্যমে কাঙ্ক্ষিত উৎপাদ পাওয়া যায়। তবে হাজারো যৌগের মাঝে কোনটা ছেড়ে কোনটা তৈরি হবে, বিষয়টা আসলেই একটু জটিলই বটে। তবে হতাশ হয়ে পড়ার কোনো কারণ নেই কারণ সবচেয়ে জটিল জিনিসের সমাধান সবচেয়ে সহজ হয়। আর যৌগের রূপান্তর নামক ভয়ংকর এই চোরাবালি থেকে বেড়িয়ে আসার উপায় হলো- যৌগ রূপান্তরের ফ্লো চার্ট (Flow chart of Conversion Reactions) । এই চার্টের মাধ্যমে খুব সহজেই এক যৌগ থেকে অন্য যৌগ তৈরির ধাপগুলো জানা যায়।
উপরের ফ্লো-চার্টটি থেকে খুব সহজেই বুঝা যায় যে কোন যৌগ থেকে কোন যৌগ উৎপন্ন সম্ভব এবং তাদের অন্তর্বর্তীকালীন উৎপন্ন হওয়া যৌগগুলো। যদিও এই ছকের বাহিরেও প্রত্যেকটি যৌগ তৈরি করার অনেক নিয়ম আছে। তবে এই ফ্লো-চার্টের মাধ্যমে আমরা ভাল একটি ধারণা পাবো জৈব রসায়নের অনেক ছোটবড় যৌগ তৈরির পদ্ধতি সম্পর্কে।
শর্টকাট: এক যৌগ থেকে অন্য যৌগ তৈরির উল্লেখিত ফ্লোচার্টটি তখনই পরিপূর্ণতা লাভ করবে যখন আমরা বিক্রিয়ার সম্পূর্ণ পদ্ধতি জানতে পারবো। চার্ট থেকে আমরা বিক্রিয়ায় অংশ নেয়া একটি বিক্রিয়কের তথ্য পেতে পারি। রাসায়নিক বিক্রিয়ায় অংশ নেয়া অপর বিক্রিয়কগুলো সম্বন্ধে জানতে পারবো নিম্নোক্ত তথ্যের মাধ্যমে,
- অ্যালকেন থেকে অ্যালকাইল হ্যালাইড ক্লোরিন যুক্ত করতে হবে (ক্লোরিনেশন)।
- অ্যালকিন থেকে অ্যালকাইল হ্যালাইড হ্যালোজেন যুক্ত করতে হবে।
- অ্যালকাইন থেকে বেনজিন (অ্যারোমেটিক যৌগ) পলিমারাইজেশন করতে হবে।
- অ্যালকাইল হ্যালাইড থেকে অ্যালকোহল পানি সংযোজন করতে হবে।
- অ্যালকাইল হ্যালাইড থেকে অ্যালকাইল সায়নাইড নাইট্রোজেন যুক্ত করতে হবে।
- অ্যালকাইল হ্যালাইড থেকে ইথার সিলভার অক্সাইড ( যুক্ত করতে হবে।
- অ্যালকাইল সায়নাইড থেকে অ্যামিন অ্যালকাইল সায়নাইড লঘু করতে হবে।
- অ্যালকোহল থেকে কার্বক্সিলিক এসিড অক্সিডেশন করতে হবে।
- প্রাইমারী অ্যালকোহল থেকে অ্যালডিহাইড কন্ট্রোল অক্সিডেশন করতে হবে।
- সেকেন্ডারি অ্যালকোহল থেকে কিটোন অক্সিডেশন করতে হবে।
- কার্বক্সিলিক এসিড থেকে এস্টার অ্যালকোহল যুক্ত করতে হবে।
- কার্বক্সিলিক এসিড থেকে অ্যামাইড অ্যামোনিয়া যুক্ত করতে হবে।
- কার্বক্সিলিক এসিড থেকে আসাইল হ্যালাইড ফসফরাস পেন্টাক্লোরাইড ( / ফরফরাস ট্রাইক্লোরাইড / থায়োনাইল ক্লোরাইড (যুক্ত করতে হবে।
- কার্বক্সিলিক এসিড থেকে অ্যানহাইড্রাইড দহন করতে হবে।
৫. উর্টজ বিক্রিয়া:
জৈব রসায়ন পড়ার সময় কোনো না কোনো পর্যায়ে এসে উর্টজ বিক্রিয়া্র নাম আমরা শুনেই থাকবো। উর্টজ বিক্রিয়ায় দেখা যায়, অ্যালকাইল হ্যালাইড বা হ্যালোঅ্যালকেন ধাতব সোডিয়ামের সাথে বিক্রিয়া করে উচ্চতর অ্যালকেন গঠন করে। এই বিক্রিয়া লেখার সময় আমাদের অনেকেরই ভুল হয়। তাই এটি মনে রাখার একটি শর্টকাট হলো,
(Source: Self illustrated)
এখানে একটি মজার ব্যাপার হলো, উৎপাদে কতগুলো অ্যালকেন তৈরি হবে তা নির্ভর করে মূল অ্যালকাইল হ্যালাইডে অ্যালকেনের সংখ্যার উপর। উৎপাদে সর্বদা মূল অ্যালকাইল হ্যালাইডের অ্যালকেনের দ্বিগুণ অ্যালকেন উৎপন্ন হবে। এখানে অনুঘটক হিসেবে উপস্থিত থাকবে শুষ্ক ইথার। এই নিয়মে বিক্রিয়কের কেবল প্রথম অ্যালকাইল হ্যালাইড ছাড়া অন্য কোনো অ্যালকাইল হ্যালাইডের সংখ্যা গণ্য করা হয় না। উক্ত সাংকেতিক বিক্রিয়ায় মূল অ্যালকাইল হ্যালাইডে একটি মাত্র অ্যালকেন রয়েছে। সুতরাং উৎপাদে তার দ্বিগুণ অর্থাৎ ২টি অ্যালকেন উৎপন্ন হবে। উপরের ছবির বিক্রিয়ার ন্যায় উৎপাদে সর্বদা সোডিয়াম ধাতুর সাথে অ্যালকাইল হ্যালাইডের হ্যালোজেন যুক্ত হবে এবং বিক্রিয়কের দুই পার্শ্ববর্তী R উৎপাদে একত্রিত হবে।
 আরো পড়ুন: এসএসসি-তে রসায়ন জয় করতে যা প্রয়োজন
আরো পড়ুন: এসএসসি-তে রসায়ন জয় করতে যা প্রয়োজন
জৈব যৌগে ভালো করার উপায়
রসায়ন বিষয়ের নামটা যতই রসালো হোক না কেনো, বিষয়টা যথেষ্ট বিভীষিকাময় বলে ধারণা আমাদের ছাত্রদের। আর জৈব রসায়ন এমন একটি অধ্যায় যা রসায়নের বিভীষিকাকে যেন নতুন এক মাত্রা দিয়েছে। আমাদের দেশের মাধ্যমিক ও উচ্চমাধ্যমিক পর্যায়ের শিক্ষার্থীদের জন্য এই বিভীষিকা যথেষ্ঠ চিন্তার কারণ।
একদিনেই জৈব রসায়নে পারদর্শিতা সম্ভব, এরকম ভাবা বোকামিই হবে। তবে নিয়মিত চর্চা আর কিছু নিয়ম অনুসরণ করে পড়তে পারলে জৈব যৌগের কনসেপ্ট ছোট্ট শিশুদের ধারাপাত বইয়ের মতই মজাদার আর সহজ হয়ে যাবে। আর তখন রসায়নকে সত্যিকার অর্থেই রসে পরিপূর্ণ বলে মনে হবে। আর দেরি না করে চলো এরকমই কিছু নিয়ম শিখে নেওয়া যাক যেগুলো জানা থাকলে জৈব রসায়নে ভালো করা সম্ভব।
১. স্রোতে গা ভাসিও না :
কেমিস্ট্রির এই জৈব রসায়ন অংশটা নিয়ে নানা ধরণের কথা শুনবে। যুগে যুগে এই বিষয়টা নিয়ে রীতিমতো ভৌতিক উপাখ্যান রচিত হয়ে আসছে। এসবে কর্ণপাত করলে বা হাইপের কারণে ভয় পেলে আদতে নিজেরই ক্ষতি হবে। আত্মবিশ্বাসী হও। তারা পারেনি বলে তুমিও পারবে না, এটা ভুল। নিজের সবটুকু দিয়ে চেষ্টা করতে হবে।

২. চাপ বিদায় করো
পড়তে বসার আগেই জৈব রসায়ন অংশের আকার দেখে ভয় পেয়ে পড়ার ইচ্ছা বিসর্জন দেওয়া যাবে না। জৈব যৌগে অনেক বেশি কিছু পড়তে হয় না। বাইরের বাড়তি জ্ঞান আরোই নিষ্প্রয়োজন। নিজের পাঠ্যবই আর গুরুত্বপূর্ণ কিছু টপিক পড়লেই পরীক্ষায় ভালো করা সম্ভব। তাই এ সংক্রান্ত ইহলৌকিক যাবতীয় চিন্তা বিদেয় দিয়ে পড়তে বসে যাও।
৩. শুধু মুখস্থবিদ্যা নয়
জৈব যৌগ সম্পর্কে আরেকটা বহুল প্রচলিত ধারণা হচ্ছে, সব অন্ধভাবে মুখস্থ করে ফেলতে হবে। এই ধারণা তোমাকে ভুল পথে পরিচালিত করবে। অস্বীকার করার উপায় নেই যে কিছু কিছু বিষয়ের সাথে মুখস্থ করার ব্যাপার আছে, কিন্তু অধিকাংশ ক্ষেত্রেই বুঝে পড়তে হবে। ঢালাওভাবে বিক্রিয়া মুখস্থ না করে বিক্রিয়ার মেকানিজম বুঝে ভেঙে ভেঙে পড়ার অভ্যাস করতে হবে।
ঘুরে এস জৈব রসায়নের জগৎ থেকে!
জৈব রসায়ন এমন একটি বিষয় যেটি অনেকের কাছেই বিভীষিকা-স্বরূপ। সঠিক পদ্ধতিতে জৈব রসায়নের অধ্যায়গুলো পড়লে বিষয়টি অনেক সহজ হয়ে যায়।
তাই আর দেরি না করে, এই প্লে-লিস্টটিতে চলে যাও সঠিক পদ্ধতিতে জৈব রসায়ন শিখতে! 😀
৪. পড়ার অভ্যাস
জৈব রসায়ন বিষয়টাতে সময় দিতে হবে। নিয়মিত রুটিন করে অল্প করে পড়তে হবে। আর বারবার সেসব অনুশীলন করতে হবে। অল্প সময় দিয়ে একবারে সব গলধকরণ করতে চাইলে আখেরে ফল ভালো হবে না কখনোই। জৈব রসায়নে ভালো করতে শুধু মেধা বা দ্রুত আত্মস্থ করার ক্ষমতা কিংবা বুঝে পড়া যথেষ্ট নয়। সময় দিয়ে রুটিন করে পড়তে হবে। সপ্তাহে নির্দিষ্ট কিছু ঘণ্টা শুধু এর জন্য আলাদাভাবে বরাদ্দ রাখো। অনেকে শুধু এর অভাবেই শেষ মূহুর্তে সব পড়তে যেয়ে ভজকট পাকিয়ে ফেলে।
৫. পর্যাপ্ত অনুশীলন
প্রচুর অনুশীলন করতে হবে। এর জন্য অনেক বেশি সমস্যা সমাধান করতে হবে। বিক্রিয়াগুলো ও যৌগগুলো বারবার লিখে লিখে আয়ত্ত্বে আনতে হবে। ক্লাসে শিক্ষকদের পড়ানো এবং বিগত বছরগুলোয় আসা প্রশ্নসমূহ বেশি গুরুত্বের সাথে পড়তে হবে। জৈব রসায়ন বিষয়টা ভালো করতে অনেক উচ্চস্তরের মেধার প্রয়োজন নেই, প্রয়োজন একটু বেশি পরিশ্রমের।
৬. মেকানিজমে গুরুত্ব দাও
বিক্রিয়া সম্পূর্ণ মুখস্থ না করে এর ভেতরের ক্রিয়াকৌশল বোঝার চেষ্টা করতে হবে। ভেঙে ভেঙে একাধিক ধাপে বিক্রিয়া বোঝার চেষ্টা করো। যা পড়ছ, বা যে বিক্রিয়াটা শিখছ, সেটার সাথে মিল আছে, এরকম বিক্রিয়াগুলো খোঁজার চেষ্টা করো। সেগুলো একসাথে পড়ার চেষ্টা করো। খাতায় আলাদাভাবে লিখে ফেল। বিক্রিয়া মুখস্থ না করে কেন এবং কিভাবে হচ্ছে, এই বিষয়ে গুরুত্ব দাও।
৭. গ্রুপে পড়তে পারো
একটা টপিক হয়তো তুমি খুব ভালো পারছ না বা বুঝতে অসুবিধা হচ্ছে। তোমার কোনো বন্ধু হয়তো সেটা ভালো পারে। ওর কাছে এটা খুব জলদি বুঝিয়ে নিতে পারবে। তাই গ্রুপ করে পড়তে পারো। আবার ধরো তুমি ভালো বুঝছ, আরেকজনকে যখন সেটা বুঝিয়ে দিতে যাবে, তোমার পড়াটা আরো একবার ঝালিয়ে নিতে পারবে। যার বা যাদের সাথে পড়তে চাও, তারা তোমার থেকে ফাস্ট বা স্লো হলে পার্টনার বদলে ফেল! তবে খেয়াল রাখবে, গ্রুপ থেকে যেন তোমার উপকার হয়, সময় নষ্ট না হয়।
জৈব রসায়ন বিষয়টাকে ভয় পাওয়া চলবে না। আবার একে কম গুরুত্ব দিলেও ঠকবে। নিয়মিত রুটিন করে অল্প অল্প পড়তে হবে। পর্যাপ্ত অনুশীলন করতে হবে। মেধা বা মুখস্থ করার শক্তি নয়, জৈব যৌগে সফলতার মূল সূত্রটা হচ্ছে নিয়মমাফিক পর্যাপ্ত অনুশীলন। রসায়নের এই অংশটুকুকে একটু সময় দাও, ভালোবাসো, আশা করি নিরাশ হবে না!
Reference:
http://organicchemistoncall.com/tag/organic-chemistry-tips-and-tricks/
https://chem.libretexts.org/Bookshelves/Organic_Chemistry/
https://www.youtube.com/playlist?list=PLpfpHUN8clmJYF9R3VCyzHrQjisrcrJht (Crash Course)
https://www.youtube.com/playlist?list=PL1pf33qWCkmgI9bgWA8qbfmzUmMvBAxxK (10 Minute School)
এইচএসসি ও এডমিশন পরীক্ষার্থীদের জন্য আমাদের কোর্সসমূহঃ
- HSC 25 অনলাইন ব্যাচ ২.০ (বাংলা, ইংরেজি, তথ্য ও যোগাযোগ প্রযুক্তি)
- HSC 26 অনলাইন ব্যাচ (বাংলা, ইংরেজি, তথ্য ও যোগাযোগ প্রযুক্তি)
- HSC 25 অনলাইন ব্যাচ (ফিজিক্স, কেমিস্ট্রি, ম্যাথ, বায়োলজি)
- HSC 26 অনলাইন ব্যাচ (ফিজিক্স, কেমিস্ট্রি, ম্যাথ, বায়োলজি)
- মেডিকেল এডমিশন কোর্স – ২০২৪
- ঢাকা ভার্সিটি A Unit এডমিশন কোর্স – ২০২৪
- ঢাকা ভার্সিটি B Unit এডমিশন কোর্স – ২০২৪
- বুয়েট কোশ্চেন সলভ কোর্স
- গুচ্ছ A Unit এডমিশন কোর্স – ২০২৪
- গুচ্ছ B Unit এডমিশন কোর্স – ২০২৪
বছরজুড়ে অভিজ্ঞ টিচারদের সাথে ক্লাস 6-10 এর পড়াশোনা ও পরীক্ষার জন্য সেরা প্রস্তুতি নিতে আজই ভিজিট করো আমাদের অনলাইন ব্যাচ ২০২৫ -এ:
১০ মিনিট স্কুলের ক্লাসগুলো অনুসরণ করতে ভিজিট: www.10minuteschool.com





আপনার কমেন্ট লিখুন